放疗基础 | 放疗术语大全(三)
百分深度剂量(percentage depth dose PDD):水模体中射线束中心轴某一深度的吸收剂量与参考深度的吸收剂量的比值。影响因素包括:射线能量,照射野,源皮距和深度。各个放疗中心应根据机型的不同具体测量和建立不同射线束的百分深度剂量数据。
组织空气比(tissue air ratio TAR):水模体射线束中心轴某一深度的吸收剂量,与空气中距离放射源相同距离处,在一刚好建立电子平衡的模体材料中吸收剂量的比值。若深度正好位于参考深度d0处,其组织空气比通常取名为反向散射因子或峰值散射因子。影响因素包括:射线能量,照射野,深度。
组织模体比(tissue phantom ratio TPR):水模中射线束中心轴某一深度的吸收剂量,与距放射源相同距离的同一位置,校准深度处吸收剂量的比值。校准深度的选择低于10MV的X线为5cm,10~25MV的X线为7cm。影响因素同TAR。
组织最大比(tissue maximum ratio TMR):水模中射线束中心轴某一深度的吸收剂量,与距放射源相同距离的同一位置,参考深度处吸收剂量的比值。影响因素同TAR。
散射空气比(scatter air ratio SAR):水模中某一深度的散射线剂量,与空间同一点空气吸收剂量的比值,等于某一点某一放射野的组织空气比减去零野的组织空气比,若该点为最大剂量点,则这时称散射最大剂量比(scatter maximun ratio SMR)。
X线百分深度剂量的影响因素:
1. 能量和深度:对于中低能X线来说,随着深度增加,百分深度剂量减小,下降速率较快;对于高能X线来说,由于剂量建成效应,百分深度剂量先增大后减小,减小的速率较慢;
2. 照射野:由于照射野中某一点的吸收剂量包有效原辐射(放射源原射线和经准直器产生的散射线)和有效原辐射在模体中产生的散射线,而高能X射线散射方向更多的是沿其入射方向向前散射,中低能X线旁向散射多见,所以,中低能X射线的百分深度剂量随照射野的变化比高能X线显著;
3. 源皮距:由于平方反比定律即近源处剂量减少的速率大于远源处的影响,所以百分深度剂量随源皮距的增加而增加。
未完待续,敬请关注……
有位老师后台留言想了解TOMO刀的知识。下面是相关介绍,供参考。
基本介绍
TOMO刀放疗英文全称Tomotherapy或Helical Tomotherapy (HT),又称螺旋断层放疗或托姆刀放疗。TOMO刀放疗是2003年正式进入临床的一种全新概念的放疗技术。这种技术使用专用的螺旋断层放疗机—Tomo刀:将一台小型化6兆伏(MV)医用直线加速器安装在螺旋CT的滑环机架上,反向利用CT成像原理,运用高能X射线进行放射治疗。
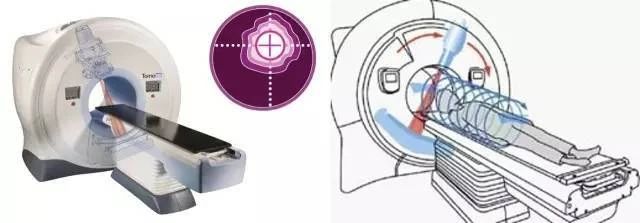
TOMO刀是CT图像引导的一种调强放疗IMRT,但和传统的直线加速器的调强放疗IMRT不太一样。主要的差异在于TOMO刀设备通过旋转机架给出窄的调强束流,而治疗床上的患者随之同步移动(如下图所示)。而传统调强放疗中,患者是静止不动的,给出的调强的束流也比较宽。TOMO刀原则上可以在人体内实现任何要求的剂量分布。从而很容易达到放射治疗的理想目标:给予肿瘤区域足够高的致死剂量,而同时最大程度降低对周边关键器官和正常组织的照射伤害。
美国放疗协会ASTRO主办的著名红皮杂志以及其他大量国际知名肿瘤专业期刊对Tomo刀各种临床应用结果都有非常详尽的比较分析和报告。其结论是:Tomo刀放疗在对绝大多数肿瘤进行放射治疗方面超越现有常规放射治疗技术,并且操作和实施较为简单。
治疗范围
具体来讲,以下肿瘤尤其适合TOMO刀放疗:
-
胶质瘤、脑转移瘤、脑膜瘤等颅内良恶性肿瘤。
-
鼻咽癌、上颌窦瘤、喉癌、舌癌等头颈部恶性肿瘤。
-
肺癌、乳腺癌、食管癌、纵隔肿瘤等胸部恶性肿瘤。
-
肝癌、胃癌、胰腺癌、胆道系统、肾脏等腹部恶性肿瘤。
-
前列腺癌、精原细胞瘤、宫颈癌、子宫内膜癌、直肠癌、膀胱癌等盆腔恶性肿瘤。
-
脂肪肉瘤、骨肉瘤、基底细胞癌、皮肤鳞癌、黑色素瘤等皮肤和软组织恶性肿瘤。
-
白血病、恶性淋巴瘤等造血系统病变。
-
各类恶性肿瘤的骨、肝、肺、淋巴结等转移性病变。
优点
1. TOMO刀适用范围广,可同时治疗任意尺寸大小、任意形状、任意部位、任意数量的肿瘤;2. 治疗时间短,出束平均在3~8分钟;3. 具有不开刀、无创伤、不打麻药等优点。4
缺点
TOMO刀疗程长,一般要在6-7周的时间里,分30-35次照射。
文章来源:本文根据网络资料整理


